Halo sahabat Latis, masih ingatkah kamu tentang senyawa karbon? Golongan hidrokarbon sendiri terdiri alkana, alkena, dan alkuna. Bila satu atau lebih atom H pada alkana diganti dengan atom atau gugus lain akan dihasilkan senyawa turunan alkana.
Yuk, hari ini kita pelajari materi kimia tentang senyawa turunan alkana, termasuk alkohol, ester, aldehid, keton, dan asam karboksilat.
Alkohol dan Eter
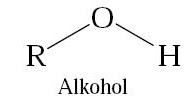
Alkohol merupakan golongan senyawa dengan rumus umum R-OH, di mana R adalah alkil (R = CnH2n+1). Dengan demikian alkohol dapat dianggap sebagai turunan dari alkana (R-H) di mana 1 atom H nya diganti dengan gugus -OH.
- Alkohol dan eter adalah senyawa yang secara struktur molekul merupakan isomer fungsional dengan rumus molekul CnH2n+2O. Perbedaan keduanya terletak pada gugus fungsionalnya yaitu gugus -OH untuk alkohol dan -OR untuk eter.
- Sifat fisika meliputi wujud yang secara umum berubah dari gas sampai padat, seiring bertambahnya jumlah atom C. Titik Didih Alkohol relatif lebih tinggi daripada eter karena alkohol memiliki ikatan hidrogen antar molekulnya. Kelarutan alkohol lebih baik daripada eter karena alkohol merupakan senyawa polar.
- Alkohol dan eter merupakan senyawa nonelektrolit.
- Sifat kimia alkohol meliputi, ikatan hidrogen, bersifat polar, secara umum dapat dioksidasi kecuali alkohol tersier. Sifat kimia yang lain meliputi beberapa reaksi diantaranya: dehidrasi dan esterifikasi.
- Sifat kimia eter meliputi senyawa sedikit polar dengan gaya antar molekul yaitu gaya Van Der Waals. Senyawa ini mudah terbakar, dapat dioksidasi menjadi keton dan dapat direduksi menjadi alkohol primer.
- Reaksi identifikasi alkohol dan eter dapat dengan menggunakan logam Na, dimana alkohol akan bereaksi sedang eter tidak bereaksi.
- Pembuatan alkohol dapat dilakukan dengan beberapa cara yaitu: − Reduksi aldehid dan keton − Hidrolisis alkil hidrogen sulfat − Hidrasi alkena. − Hidrolisis ester.
- Pembuatan alkohol menggunakan reagen Grignard.
- Eter dibuat dengan sintesis eter Williamson.
- Kegunaan alkohol dalam kehidupan lebih banyak digunakan sebagai pelarut, sedangkan eter digunakan sebagai zat anestetik.
Aldehid dan Keton
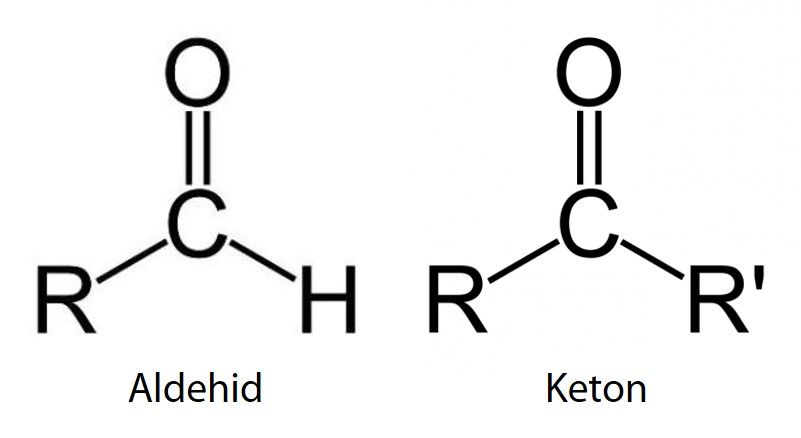
Aldehid dan keton adalah senyawa yang secara struktur molekul merupakan isomer fungsional dengan rumus molekul CnH2nO. Perbedaan keduanya terletak pada gugus fungsionalnya yaitu gugus -CHO untuk aldehid dan -OR untuk keton.
- Sifat fisika meliputi wujud yang secara umum berubah dari gas sampai cair, seiring bertambahnya jumlah atom C. Keduanya merupakan senyawa polar.
- Sifat kimia aldehid meliputi, bersifat polar, secara umum dapat dioksidasi menjadi asam karboksilat. Sifat kimia yang lain adalah positif terhadap uji Fehling dan Tollens yang membedakan dengan keton.
- Keton dapat dioksidasi menjadi ester dan dapat direduksi menjadi eter. Berbeda dengan aldehid senyawa golongan ini negatif terhadap uji Fehling dan Tollens.
- Pembuatan aldehid dapat dilakukan dengan beberapa cara yaitu: a. Oksidasi alkohol primer. b. Reduksi asam karboksilat c. Keton dibuat dengan oksidasi alkohol sekunder
- Kegunaan aldehid dalam kehidupan lebih banyak digunakan dalam dunia kedokteran sebagai pengawet preparat ataupun jenazah, sedangkan keton banyak digunakan sebagai pelarut dan bahan baku dalam industri.
Asam Karboksilat dan Ester

- Asam karboksilat dan ester adalah senyawa yang secara struktur molekul merupakan isomer fungsional dengan rumus molekul CnH2nO2. Perbedaan keduanya terletak pada gugus fungsionalnya yaitu gugus -COOH untuk asam karboksilat dan -COOR untuk ester.
- Sifat fisika meliputi wujud yang secara umum berubah dari cair, kental sampai padat, seiring bertambahnya jumlah atom C. Titik didih asam karboksilat relatif tinggi, karena mempunyai ikatan hidrogen yang lebih kuat bahkan dari alkohol sesukunya. Titik didih ester relatif rendah karena tidak memiliki ikatan hidrogen. Asam karboksilat dan ester keduanya dapat larut merupakan senyawa polar, kecuali ester pada suku yang tinggi. Asam karboksilat adalah elektrolit lemah, sedangkan ester merupakan nonelektrolit.
- Sifat kimia asam karboksilat meliputi, ikatan hidrogen, bersifat polar, dan dapat direduksi menjadi aldehid. Sifat kimia yang popular adalah esterifikasi dan penyabunan.
- Sifat kimia ester meliputi senyawa sedikit polar dengan gaya antar molekul yaitu gaya Van Der Waals. Senyawa ini bersifat kurang reaktif.
- Reaksi identifikasi alkohol dan eter dapat dengan menggunakan uji sifat asam dengan menggunakan indikator asam basa.
- Pembuatan asam karboksilat dapat dilakukan dengan oksidasi berlanjut alkohol primer menggunakan oksidator kuat KMnO4, sedang pembuatan ester dengan reaksi esterifikasi.
- Kegunaan asam karboksilat sangat luas mulai dari zat tambahan masakan atau makanan sampai pelarut dalam dunia industri. Kegunaan ester lebih dikenal dalam perisa makanan aroma buah-buahan dan lilin atau wax.
Baca juga: Blog Supercamp Alumni UI
Gimana sobat, udah mulai paham kan dengan materi ini? Supaya kamu makin paham dengan materi lainnya, bisa jawab PR dan tugas di sekolah dengan mudah dan prestasimu meningkat tajam, kamu bisa coba ikutan les privat Latiseducation lho.. gurunya bagus-bagus dan biayanya hemat. Bisa online dan tatap muka juga
Nah, itulah pembahasan materi kali ini. Apabila ada pertanyaan atau pendapat yang ingin disampaikan, Anda bisa langsung serukan di kolom komentar di bawah yaaaah…
Anda juga dapat menghubungi kami di 085810779967 atau Head Office kami 021-77844897 di setiap hari Senin s.d Jumat pada pukul 09.00-17.00.
Anda bisa menemui kami langsung di kantor Ocean Terrace Residence Blok E1 No.1 Jalan Tole Iskandar, Tirtajaya, Kec. Sukmajaya, Kota Depok, Jawa Barat. Latis Education melayani les privat untuk semua wilayah di Indonesia.
Sumber: Repositori Kemdikbud